
گروه 16 جدول تناوبی مندلیف، از پنج عنصر به شرح زیر تشکیل شده است:
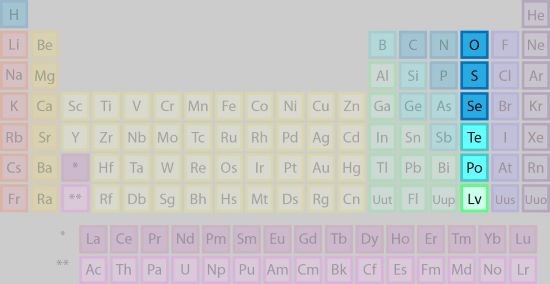
از آنجایی که بسیاری از این عناصر را میتوان از کانیهای سولفیدی یا اکسیدی استخراج کرد، عناصر این گروه به عنوان کالکوژن یا عناصر سنگ ساز نیز شناخته میشوند. در میان این عناصر، اکسیژن فراوانترین آنها در سیاره زمین است. هنگامی که نسبت انواع مختلف اتمهای موجود در جهان محاسبه شد، اکسیژن به عنوان چهارمین عنصر فراوان پس از هیدروژن، هلیوم و نئون اعلام شد. به طوری که این عنصر حدود 89% از آب، 46% از پوسته زمین و 20% از هوا را تشکیل میدهد. برای آشنایی بیشتر با مشخصات و کاربردهای گاز اکسیژن، مطالعه این مقاله را به شما پیشنهاد می دهیم.
خواص اکسیژن با سایر عناصر هم گروه خود بسیار متفاوت است؛ اما همه آنها دارای 2 الکترون در لایه اوربیتال s بیرونی و 4 الکترون در لایه اوربیتال p هستند که معمولا به صورت s2p4 نوشته میشود.
پیکربندی الکترون برای هر عنصر در زیر آورده شده است:
روند خواص دورهای عناصر در این گروه بسیار جالب است. دانستن این روند به ما این امکان را میدهد که نحوه و میزان واکنش عناصر گروه خانواده اکسیژن را با عناصر دیگر پیش بینی کنیم. بیشتر این روندها، برای تمامی گروههای دیگر عناصر صادق است. این روندها در زیر توضیح داده شده است:

اکسیژن که با علامت شیمیایی O نشان داده میشود، یک گاز بی رنگ و بی بو است که در طی فرآیند تنفس انسان و سایر جانوران به دی اکسید کربن تبدیل میشود. گاز اکسیژن یک مولکول دو اتمی است که در مقادیر کم نیز به عنوان یک مولکول سه اتمی (O3) یافت میشود که به اوزون معروف است.
بسیاری از عناصر شناخته شده، به راحتی با اکسیژن ترکیب میشوند که انرژی گرمایی زیادی در طول این ترکیب آزاد میشود؛ این فرآیند به عنوان احتراق نیز شناخته میشود. اما از طرفی دیگر، اکسیژن را میتوان به صورت خالص به شکل کپسول گاز اکسیژن ذخیره سازی کرد.
نماد S نشان دهنده عنصر گوگرد است. گوگرد یک نافلز است که از نظر فراوانی در جهان، در رتبه نهم قرار دارد. گوگرد را میتوان در هر دو حالت ترکیبی و آزاد یافت. سولفاتها، در حدود 0.09 درصد از میزان گوگرد موجود در آب دریا و اقیانوس را تشکیل میدهند. گوگرد در محیطهای ذکر شده، در اثر باکتریهای بی هوازی روی کانیهای سولفاتی مانند گچ تشکیل میشود.
سلنیوم کمیابتر از اکسیژن یا گوگرد است. میتوان این عنصر را در چند ماده معدنی هم به صورت آزاد و هم به صورت ترکیب با فلزات سنگین (مانند سرب، نقره یا جیوه) پیدا کرد. در حالت معمول، شکل فلزی و خاکستری سلنیوم، پایدارترین شکل عنصر است.
تلوریم عنصر شیمیایی با عدد اتمی 52 و خواصی بین فلزات و نافلزات است. این عنصر، یکی از نادرترین عناصر پایدار پوسته زمین است و اغلب در حالت آزاد و همچنین در ترکیباتی با عناصری مانند مس، سرب، نقره و طلا یافت میشود.

نادرترین عنصر در گروه خانواده اکسیژن، پولونیوم است. این عنصر یک ماده رادیواکتیو است؛ به طوری که گاهی اوقات در کاربردهای پرتو آلفا در آزمایشهای علمی استفاده میشود.
شعاع اتمی یا شعاع یونی عناصر گروه خانواده اکسیژن، با پیشروی در این گروه افزایش مییابد. کمترین شعاع اتمی و یونی مربوط به اکسیژن است، در حالی که کالکوژن با بزرگترین شعاع (به استثنای لیورموریوم) پلونیوم است. قابل ذکر است که افزودن پروتونها و افزایش بار موثر هستهای باعث میشود که شعاع اتمی عناصر در طول زمان کاهش پیدا کند. به طوری که شعاع اتمی اکسیژن بسیار کوچکتر از لیتیوم میشود.
آنتالپی افزایش الکترون در این عناصر، با افزایش اندازه اتم کاهش مییابد. در نتیجه، آنتالپی افزایش الکترونی کالکوژنها با حرکت به سمت پایین گروه کاهش پیدا میکند. شایان ذکر است که اکسیژن آنتالپی الکترون منفی کمتری نسبت به گوگرد دارد. میتوان آن را به ساختار اتمی فشرده اکسیژن نسبت داد که به دافعه بین الکترونی بین الکترونهای ظرفیت و هر الکترون نزدیک دیگری کمک میکند.
الکترونگاتیوی عناصر گروه خانواده اکسیژن با حرکت به سمت پایین در این گروه به دلیل عوامل مختلفی از جمله افزایش شعاع اتمی و افزایش دافعه الکترون-الکترون کاهش مییابد. الکترونگاتیوترین کالکوژن اکسیژن است و کمترین الکترونگاتیوی کالکوژن پلونیوم است (لیورموریوم در نظر گرفته نمیشود).
عناصر غیر فلزی گروه خانواده اکسیژن، شامل اکسیژن و گوگرد میشود. شبه فلزها شامل سلنیوم و تلوریم هستند. و در آخر، پلونیوم یک عنصر رادیواکتیو دارای خواص فلزی است.
نقطه ذوب و نقطه جوش عناصر گروه خانواده اکسیژن، با پیشروی آنها در یک گروه به دلیل افزایش اندازه اتمی و جرم اتمی (در نتیجه افزایش نیروهای جاذبه بین مولکولی) افزایش مییابد. در بین کلکوژنها، اکسیژن کمترین نقطه ذوب و جوش را دارد. تفاوت قابل توجه میان نقطه ذوب و جوش گوگرد و اکسیژن را میتوان به این واقعیت نسبت داد که اکسیژن در جو به عنوان یک مولکول دو اتمی وجود دارد، در حالی که گوگرد معمولاً به عنوان یک مولکول چند اتمی یافت میشود.
تقریبا تمامی عناصر گروه خانواده اکسیژن دارای آلوتروپهای متعدد هستند. در واقع، 9 آلوتروپ شناخته شده از اکسیژن وجود دارد که رایجترین آنها، دیاکسیژن و ازن هستند..
علاوه بر این، بیش از 20 آلوتروپ شناخته شده از گوگرد وجود نیز دارد. گوگرد مونوکلینیک و گوگرد لوزی دو شکل آلوتروپیک پایدار گوگرد هستند. گوگرد مونوکلینیک و گوگرد لوزی دو شکل آلوتروپیک پایدار گوگرد هستند.
سلنیوم نیز دارای پنج آلوتروپ مختلف است؛ در حالی که پلونیوم دارای دو نوع است.
از آنجایی که آرایش الکترونی کلی عناصر گروه خانواده اکسیژن ns2 np4 است، میتوانند با به دست آوردن دو الکترون یا مشارکت در پیوند کووالانسی، به آرایش الکترونی پایداری دست یابند. هنگامی که این عناصر دو الکترون به دست میآورند، یونی با فرمول کلی M-2 تشکیل میدهند (M نشان دهنده یک کالکوژن است). کالکوژنها حالتهای اکسیداسیون 2-، 2+، 4+ و 6+ را دارند.


نگاهی به ضرورت بازنمایی رشادتهای عملیات بیتالمقدس در قالب ادبیات مدرن



گفت و گوی اختصاصی جام جم آنلاین با حسن روشن

ناصر ابراهیمی در گفت وگو با جام جم آنلاین ؛

