ارتباط باکتری های روده با بیماری های عصبشناختی
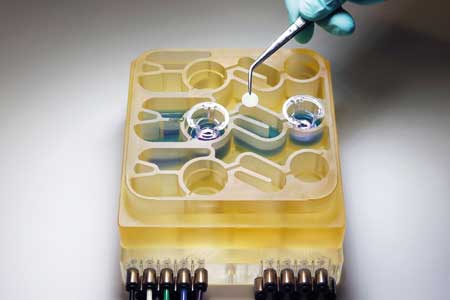
این سیستم همچون یک اندام مصنوعی کوچک است. بهتازگی محققان با استفاده از این سیستم نشان دادهاند باکتریهای موجود در مجرای گوارشی انسان چگونه موجب بیماریهای عصبشناختی میشود.
مغز و دستگاه گوارش ما به روشهای متعددی با یکدیگر ارتباط عمیقی دارند. وقتی فردی عصبی میشود، ممکن است معده او درد بگیرد.
همچنین علائم ارسالی از روده بهدلیل گرسنگی، فرد را تحریکپذیر و حساس میکند. در بررسیهای اخیر مشخص شدهاست، باکتریهایی که در روده ما ساکن هستند، موجب بروز برخی بیماری های عصب شناختی در بدن میشوند.
مدلسازی این فعل و انفعالات پیچیده در حیواناتی مانند موشها به دلیل اینکه آنها از لحاظ فیزیولوژی با انسان بسیار فرق دارند، دشوار است.
محققان دانشگاه امآیتی برای کمک به درک بهتر محور روده و مغز، سیستمی به نام «اندام تراشه» طراحی کردهاند که تعاملهای بین مغز، کبد و روده را بازتولید میکند.
آنها با استفاده از این سامانه توانستهاند اثری را که میکروبهای ساکن روده روی بافتهای سالم مغز و همچنین بافتهای گرفتهشده از یک بیمار مبتلا به پارکینسون میگذارند مدلسازی کنند.
این محققان در مطالعات خود دریافتند اسیدهای چرب زنجیره کوتاهی را که میکروبها در روده تولید میکنند و سپس به مغز فرستاده میشوند اثرات بسیار متفاوتی روی سلولهای سالم و همچنین بیمار مغزی میگذارند.
بنابه گفته مارتین تریپکار (Martin Trapecar)، یکی از محققان این پروژه در امآیتی، با اینکه اسیدهای چرب زنجیره کوتاه برای سلامت انسان بسیار مفیدند، مشخص شده این اسیدها در بیماریهای خاص، مانند پارکینسون، بروز برخی آسیبشناسیهای مغزی، مانند تاشدگی پروتئین و مرگ سلولهای عصبی را تشدید کنند.»
سیستمهای میکروفیزیولوژیک
چند سال است در آزمایشگاه لیندا گریفیث (Linda Griffith) روی تولید سیستمهای میکروفیزیولوژیک کار و تحقیق میشود. لیندا گریفیث، از استادان و محققان دانشگاه امآیتی است. سیستمهای میکروفیزیولوژیک از ابزارهای کوچکی تشکیل شده که برای رشد مدلهای بافتی مهندسیشده اندامهای متفاوت استفاده میشود. این ابزارها با کمک کانالهای ریزسیال به یکدیگر متصل شدهاند.
این سیستمها در برخی موارد بهتر از مدلهای حیوانی میتوانند اطلاعات دقیقتری از بیماریهای انسانی به دست دهند.
در بررسی سال گذشته، محققان آزمایشگاه گریفیث پس از مدلسازی تعاملهای بین کبد و روده دریافتند اسیدهای چرب زنجیره کوتاه، مولکولهایی که میکروبها آنها را در روده تولید میکنند، التهاب خودایمنی ناشی از کولیت زخمی را بدتر میکنند.
در عین حال این نوع اسیدهای چرب حاوی بوتیرات، پروپیونات و استات هستند که اثرات مفیدی روی بافتها از جمله، افزایش تحمل ایمنی بدن دارند و همچنین این اسیدها هستند که ۱۰درصد انرژی و نیرویی که از غذا میگیریم را تامین میکنند.
این تیم تحقیقاتی امآیتی در یک بررسی جدید تصمیم گرفتند مغز و سلولهای ایمنی در حال گردش در بدن را به سیستم چنداندامی آزمایشگاهی خود اضافه کنند. مغز با مجرای گوارشی در تعاملهای بسیاری است که این تعامل از طریق سیستم عصبی رودهای یا سلولهای ایمنی در حال گردش، مواد مغذی و هورمونهای بین اندامها صورت میگیرد.
چند سال قبل، یکی از استادان و محققان میکروبیولوژی در موسسه فناوری کالیفرنیا (Caltech)، در بررسیهای خود روی موشها ارتباطی بین اسیدهای چرب زنجیره کوتاه و بیماری پارکینسون پیدا کردهبود. او آن موقع نشان دادهبود این اسیدها سرعت پیشرفت بیماری را افزایش میدهند.
در واقع وقتی باکتریها، فیبر هضمنشده در روده را مصرف میکنند، این اسیدهای چرب زنجیره کوتاه تولید میشوند. سرعت رشد بیماری این موشها اگر در محیطزیستی بدون میکروب نگهداری شوند، بسیار کاهش مییابد.
محققان امآیتی تصمیم گرفتند با استفاده از سیستم میکروفیزیولوژیک خود، نتایج این محقق را بررسی کنند.
به این منظور آنها با محققان آزمایشگاهی در موسسه وایتهد، همکاری کردند. این موسسه در گذشته با ابداع روشی، سلول های فیبروبلاست از بیماران پارکینسون را به سلولهای بنیادی پلوریپوتنت (pluripotent) منتقل کردهبود و در نتیجه فیبروبلاستها به انواع سلولهای مغزی عصبها، آستورسیتها و میکروگلیاها تبدیل شدهبودند.
بیش از ۸۰ درصد موارد ابتلا به پارکینسون را نمیتوان به جهشهای ژنتیک خاصی ارتباط داد، اما در باقی موارد جهشهای ژنتیک خاصی رخ میدهد.
سلولهایی که محققان امآیتی برای مدل پارکینسون خود استفاده کردند، حاوی جهشی بودند که موجب انباشت پروتئینی به نام آلفا سینوکلئین میشود.
این پروتئین به سلولهای عصبی صدمه زده و سلولهای مغزی را ملتهب میکند. همچنین در موسسه وایتهد، نوعی سلولهای مغزی تولید شدهبود که این جهشها را اصلاح میکرد اما آن سلولها یکسان و مشابه و فقط از یک بیمار گرفته شدهبودند.
محققان امآیتی، ابتدا دو مجموعه از سلولهای مغز سیستمهای میکروفیزیولوژیک را که بههیچیک از بافتهای دیگر متصل نبودند، بررسی کردند و دریافتند سلولهای فرد مبتلا به پارکینسون بیش از سلولهای یک فرد سالم ملتهب هستند. همچنین سلولهای پارکینسون توانایی سوختوساز لیپیدها (چربیها) و کلسترول را ندارند.
اثرات متضاد
محققان در ادامه بررسیهای خود با استفاده از سلولهای ایمنی و مواد مغذی، سلولهای مغز را به نمونههای بافتی روده و کبد متصل کردند. آنها این کار را با استفاده از کانالهایی انجام دادند که به سلولهای ایمنی و مواد مغذی اجازه عبور میداد.
در این میان اسیدهای چرب زنجیره کوتاه هم جریان یافته و به رشد سلولها کمک میکردند. اما وقتی سلولهای مغز بیماران مبتلا به پارکینسون در معرض این اسیدهای چرب قرار گرفتند، تمام فواید خود را از دست دادند و بهجای آن تاشدگی پروتئین و مرگ سلولی بیشتری رخ داد.
این وضعیت حتی زمانی که سلولهای ایمنی از سیستم حذف شدند هم مشاهده شد و محققان به این نتیجه رسیدند تغییرات در سوختوساز چربی منجر به این وضعیت میشود.
در واقع آنها میگویند، به نظر میرسد اسیدهای چرب زنجیره کوتاه بهجای اینکه تاثیر مستقیمی روی جمعیت سلولهای ایمنی خاصی داشتهباشد، روی سوختوساز لیپیدها اثر میگذارد و منجر به بیماریهای تخریبکننده عصبی میشود.
این محققان همچنین درنظر دارند انواع دیگر بیماریهای عصبشناختی را که تحت تاثیر میکروبیومهای روده قرار دارند با استفاده از سیستم اندامها روی تراشه بررسی کنند.
مترجم: نادیا زکالوند - دانش / روزنامه جام جم
منبع: Medicalxpress

تازه ها
گوناگون




مرور بزرگ ترین جنجال های تاریخ جام جهانی (8)



















